Kako bioslični lijekovi dobivaju odobrenje
Bioslični lijekovi prolaze skraćen obavezni razvojni put1–3
Tvrtka Fresenius Kabi razumije važnost biosličnih lijekova i predana je učinkovitom i sigurnom liječenju bolesnika. FDA i EMA zahtijevaju da bioslični lijekovi prođu niz strogih testova prije nego dobiju odobrenje. Specifične sličnosti s referentnim lijekom moraju se dokazati u sljedećim ispitivanjima:
Analitička ispitivanja: dokazuju da bioslični proizvodi tvrtke Fresenius Kabi imaju slične molekularne i funkcionalne karakteristike kao i odobreni lijek.
Klinička ispitivanja: jasno dokazuju djelotvornost, sigurnost, farmakokinetiku i farmakodinamiku slične onima odobrenog lijeka u najboljoj ciljnoj populaciji i indikaciji.
Razvoj biosličnih lijekova1–3
Pokazuju veliku sličnost molekule s originalnim lijekom
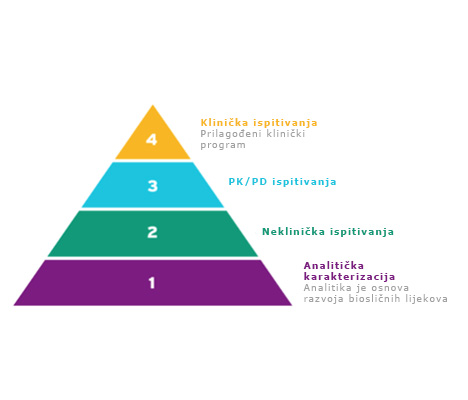
Za bioslične lijekove naglasak je na početnim fazama razvoja, s više prilagođenim programom kliničkog ispitivanja.
Bioslični lijekovi prolaze skraćeni obavezni razvojni put. Ako se za neki biosličan lijek dokaže da je biološki sličan referentnom lijeku, tada je znanstveno opravdano osloniti se na određena postojeća znanja o sigurnosti i djelotvornosti referentnog lijeka kako bi se poduprlo odobrenje.3
Skraćeni obavezni razvojni put pruža mogućnost bržeg i jeftinijeg programa razvoja biološki sličnog lijeka.3
„Dokazi prikupljeni tijekom 10 godina kliničkog iskustva pokazuju da se bioslični lijekovi koje je odobrila EMA mogu koristiti sigurno i učinkovito u svim njihovim odobrenim indikacijama kao i drugi biološki lijekovi.“1 – EMA
„Svi biološki lijekovi koje je odobrila FDA, uključujući referentne lijekove i bioslične lijekove, prolaze rigoroznu evaluaciju kako bi bolesnici mogli biti sigurni u djelotvornost, sigurnost i kvalitetu ovih proizvoda.“3 – FDA
EMA
EU je odobrila svoj prvi biosličan lijek 2006. godine. U EU-u biološke lijekove mora odobriti EMA kroz svoj „centralizirani postupak“.1 EMA-in pregled dovodi do „znanstvenog mišljenja“, koje se zatim šalje Europskoj komisiji, koja u konačnici može dati odobrenje za stavljanje u promet unutar EU-a.1
Prema EMA-inu procesu davanja odobrenja, razvoj biosličnog lijeka u velikoj se mjeri oslanja na „ispitivanja usporedivosti“ kojima se utvrđuje biosličnost s referentnim lijekom. To uključuje usporedbu (head-to-head) biosličnog lijeka i referentnog proizvoda.1 Ona se izvodi putem procesa u koracima koji se prilagođava prema svakom pojedinačnom proizvodu: znanje iz početnih ispitivanja usporedivosti kvalitete (1. korak) koristi se da bi se identificirao stupanj i vrsta nekliničkih (2. korak) i kliničkih (3. korak) ispitivanja potrebnih u sljedećem razvojnom koraku, s ciljem isključivanja razlika u performansama između predloženog biološki sličnog i referentnog lijeka.1
Tri ključna koraka na kojima se temelji razvoj biosličnih lijekova u EU-u1
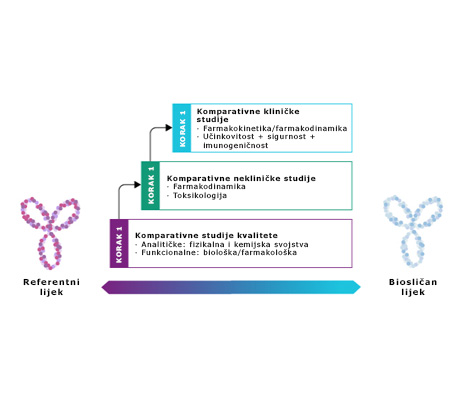
Američka FDA
Svojim Zakonom o cjenovnoj konkurenciji i inovaciji bioloških lijekova (Biologics Price Competition and Innovation Act, BPCI) iz 2009. godine američki Kongres kreirao je skraćeni put registriranja bioloških lijekova koji su dokazano biološki slični ili međusobno zamjenjivi s biološkim lijekom koji je FDA već odobrila.4 Ovaj skraćeni put dobivanja registracije osmišljen je kao način pružanja više opcija liječenja bolesnicima i povećavanja dostupnosti lijekova koji spašavaju živote i mogu smanjiti troškove u zdravstvu.4
Zahtjev za odobrenje biosličnog ili međusobno zamjenjivog lijeka mora uključivati podatke koji dokazuju biološku sličnost s referentnim lijekom. To obično uključuje podatke iz:
- analitičkih ispitivanja: koja dokazuju da je biološki lijek vrlo sličan referentnom lijeku, unatoč manjim razlikama u klinički inaktivnim komponentama3
- ispitivanja na životinjama, uključujući ispitivanje toksičnosti3
- kliničkog ispitivanja (ili više njih) koje dokazuje sigurnost, čistoću i potenciju predloženog biosličnog lijeka u jednoj ili više indikacija za koje je referentni lijek registriran. To obično uključuje ispitivanje imunogenosti, farmakokinetike te, u nekim slučajevima, farmakodinamike, a također može uključivati i komparativno kliničko ispitivanje3
Osim gore navedenoga, zahtjev za odobrenje međusobno zamjenjivog lijeka također mora uključivati informacije ili podatke koji dokazuju da:
- za predloženi međusobno zamjenjiv proizvod očekuje se da će imati isti klinički rezultat kao i referentni lijek u bilo kojeg bolesnika3
- za lijek primijenjen više od jedanput istom bolesniku, prelazak s predloženog međusobno zamjenjivog lijeka i referentnog lijeka ne dovodi do povećanih sigurnosnih rizika niti do smanjene učinkovitosti u odnosu na primjenu referentnog lijeka bez prelaska s jednog na drugi lijek3
Koncept ekstrapolacije5–7
Ekstrapolacija se odnosi na odobrenje biosličnog lijeka za indikaciju za koju nije ispitan u kliničkim ispitivanjima, a na temelju prethodne kliničke procjene i odobrenja referentnog lijeka za tu indikaciju.5–7 To znači da je potrebno provesti manje kliničkih ispitivanja ili ih uopće nije potrebno provesti na biosličnom lijeku za određene indikacije,5 čime se ubrzava proces dobivanja odobrenja i bolesnicima omogućuje pristup većem broju opcija liječenja.
Ekstrapolacija indikacija za bioslične lijekove5–7
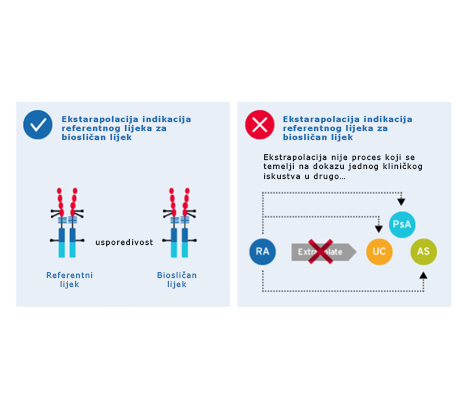
Zašto odabrati bioslične lijekove sada i u budućnosti? Saznajte ovdje
WEB-BIO-2019-04
Reference i fusnote:
EMA, Europska agencija za lijekove (European Medicines Agency); FDA, američka Uprava za hranu i lijekove (Food and Drug Administration)
1. European Medicines Agency. Biosimilars in the EU: Information guide for healthcare professionals. 2017. Dostupno na:
http://www.ema.europa.eu/docs/en_GB/document_library/Leaflet/2017/05/WC500226648.pdf (Pristup: veljača 2019.).
2. McCamish M, Woollett G. Clin Pharmacol Ther 2012; 91:405–417.
3. US Food and Drug Administration. Biosimilar development, review and approval. 2017. Dostupno na linku (Pristup: veljača 2019.).
4. US Food and Drug Administration. Biosimilars. 2018. Dostupno na linku (Pristup: veljača 2019.).
5. Mellstedt H et al. Ann Oncol 2008; 19:411–419.
6. Weise M et al. Blood 2012; 120:5111–5117.
7. European Medicines Agency. Guideline on similar biological medicinal products containing monoclonal antibodies – non-clinical and clinical issues. 2012. Dostupno na linku (Pristup: veljača 2019.).
