Biosimilaires

Un biosimilaire est un médicament biologique hautement similaire à un autre médicament biologique déjà approuvé en Europe par l’agence européenne du médicament (EMA). 1
Chaque biosimilaire autorisé en Europe présente un profil de qualité, de sécurité et d’efficacité comparable à celui de sa spécialité de référence et, comme pour celle-ci, un rapport bénéfice/risque favorable. 2
Nous nous appuyons sur notre expertise mondiale en matière de fabrication et de biotechnologie dans le but d’obtenir une grande similitude avec le traitement biologique de référence.
Fresenius Kabi est reconnu pour sa production de produits de santé couvrant une grande variété de domaines thérapeutiques, notamment dans les médicaments injectables, les formulations complexes et les dispositifs médicaux.
Nous nous appuyons sur 70 sites de production à travers le monde, nous permettant de garantir une solide chaîne de production. C'est l'une des raisons pour lesquelles nous sommes reconnus comme un partenaire fiable par les professionnels de santé.
Fort de notre expérience internationale dans la mise à disposition de produits pharmaceutiques et de dispositifs médicaux à haute valeur ajoutée, nous nous engageons dans le développement de biosimilaires dans les domaines de l'oncologie et des maladies auto-immunes.
En 2017, nous avons acquis le portefeuille de biosimilaires de Merck KGaA, doté d’un savoir-faire de plus de 20 ans dans les biotechnologies. Dans la continuité de notre recherche d'excellence dans la qualité, les biosimilaires Fresenius Kabi sont fabriqués en Europe dans le respect des lignes directrices réglementaires et des BPF (Bonnes Pratiques de Fabrication).
Un engagement à long terme en immunologie et en oncologie
L’engagement à long terme dans le développement de biosimilaires illustre la raison d’être de Fresenius Kabi « Prendre soin de la vie des patients sévères ou chroniques ».
Nous avons plusieurs molécules en cours de développement clinique, dans les domaines des maladies auto-immunes et de l’oncologie.
Membre de Medicines for Europe
Fresenius Kabi est un membre actif de Medicines for Europe, l’association européenne pour les médicaments génériques et les biosimilaires. Concrètement, cet engagement signe, pour les sociétés membres, la volonté de faciliter l’accès des patients aux médicaments et d’améliorer les solutions thérapeutiques qui leur sont proposées.

KabiCare : Programme de soutien aux patients Fresenius Kabi
Notre mission consiste à collaborer étroitement avec les professionnels de la santé, les payeurs et les patients afin de développer des services à valeur ajoutée pour améliorer les soins aux patients.
Au-delà de la qualité de notre offre produits, nous nous engageons à accompagner les professionnels de santé ainsi que leurs patients à toutes les étapes de leur parcours de soin en mettant en place un plan d’accompagnement, KabiCare.
La première étape de ce plan d’accompagnement est d’accompagner les patients sur le plan nutritionnel.

En savoir plus sur les biosimilaires
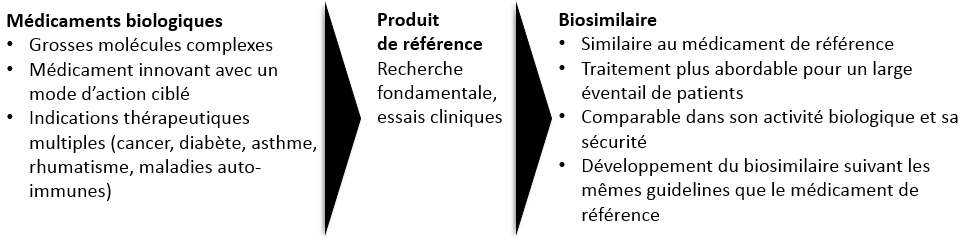
- Du médicament biologique au biosimilaire
- L’intérêt des biosimilaires
Les biosimilaires représentent une économie financière pour les systèmes de santé sans compromis sur la qualité, l’efficacité et la sécurité des produits. Ces économies réalisées contribuent à optimiser la qualité de prise en charge des patients tout en limitant les dépenses financières3 et encouragent les industries pharmaceutiques à innover et à développer de nouvelles molécules.4
Sources
- European Medicines Agency (2017) Biosimilars in the EU: Information guide for healthcare professionals. viewed on 13.03.19 http://www.ema.europa.eu/docs/en_GB/document_library/Leaflet/2017/05/WC500226648.pdf
- ANSM. États des lieux sur les médicaments biosimilaires. Mai 2016.
- Beck M. Enjeux économiques et de santé publique. Séminaire « Les médicaments biosimilaires… à vos marques prêts, prescrivez ! » ARS grand Est, janvier 2018. Accessible à l’adresse : https:// www.grand-est.ars.sante.fr/system/fi les/2018-04/23032018_Synth%C3%A8se%20s%C3%A9minaire%20biosimilaires.pdf ; accédé le 15.05.19
- Beck M, Michel B, Rybarczyk-Vigouret MC, Leveque D, Sordet C, Sibilia J, Velten M. Les médicaments biosimilaires : quels enjeux pour les professionnels de santé ? 2016 ; 22(6) : 354-63 1-10 doi:10.1684/met.2016.0595
